- Matéria: é tudo aquilo que ocupa lugar no espaço
- Massa: é a energia condensada de matéria.Quantidade de matéria existente em um corpo.
Obs: Através de uma balança você pode achar a massa de um corpo se comparando esse a massa desse corpo com uma massa tida como padrão
Obs: Se caso na questão vier dado massa, você poderá somar normalmente as duas! Porém, se na questão estiver dando os volumes, você não poderá fazer a mesma coisa.
Exemplo: Se você tiver 50 ml de água + 50 ml de etanol = 97 ml , em vez de dar 100 ml como o esperado, dá-se 97 ml, isso ocorre por causa das pontes de hidrogênio que ocasionam uma pequena interação.
PROPRIEDADES DA MATÉRIA:
- Gerais: ocorrem para todas as matérias, independente da substância que ela é formada.
Extensão
Compressibilidade
Indestrubilidade
Divisibilidade
Inércia
Elasticidade
Impenetrabilidade
- Específicas: variam de acordo com a substância que aquele corpo é constituído, logo,não são iguais para todos os corpos.
A) Organolépticas:
Cor,Brilho,Sabor e Odor
B)Não Organolépticas:
Dureza (resistência ao risco)
Tenacidade (resistência a pancada)
Maleabilidade (pode ser maleável)
Ductilidade (pode formar fios)
Densidade:
Razão entre massa e volume;Para um corpo flutuar e afundar NÃO depende da massa e sim da densidade,logo, o mais denso afundo e o menos denso flutua.
Magnetismo (ser atraído por imã):
- FERROMAGNÉTICO
Adquire campo magnético no mesmo sentido que o imã, mas o campo permanece mesmo quando o imã for removido.É chamado de MEMÓRIA MAGNÉTICA.
- PARAMAGNÉTICO
Estrutura com pelo menos um elétron desemparelhado;Pode ser atraído por imã;Campo magnético alinhado com o imã
- DIAMAGNÉTICO
Estrutura com todos os elétrons emparelhados;Não pode ser atraído por imã;Campo magnético no sentido contrário do imã.
ESTADOS FÍSICOS DA MATÉRIA:
Depende do grau de agregação entre as partículas, apresentando uma estrutura molecular definida obedecendo a teoria cinética(movimento).
- Um líquido vira vapor em qualquer temperatura,ou seja, não é necessário que se atinja 100 graus Celsius para virar vapor,obrigatoriamente. Por exemplo, ao se estender uma roupa no varal, você não espera que a água na roupa atinja temperatura de ebulição não é mesmo ?
- Um líquido começa a entrar em ebulição (aparecer aquelas bolhinhas), quando a Pressão de vapor se igualar com a Pressão atmosférica (ATM).
- O sólido é uma estrutura internamente organizada porém, existem dois tipos de sólidos, o CRISTALINO, com estrutura interna organizada e o AMORFO, chamado de FALSO SÓLIDO, por que externamente é organizado porém, internamente não, como o caso do vidro (SiO2).
Obs: Vidros tipo cristal, foram resfriados mais lentamente, tendo a oportunidade de se organizar estruturalmente se comparado aos outros vidros.
- LIOFILIZAÇÃO, é o processo de desidratação com o objetivo de se obter o pó sem perder os nutrientes. Congela, coloca em uma câmara a vácuo, abaixa-se a pressão ocorrendo a sublimação do líquido. (Exemplo: Leite em pó, Café)
Obs: Para água o aumento da pressão favorece a fusão do gelo, esse fenômeno foi explicado por Tyndall. Graças isso, você pode patinar no gelo!
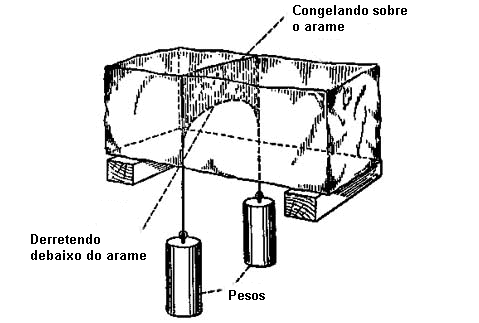 (experimento de Tyndall)
(experimento de Tyndall)


0 comentários:
Postar um comentário